INFORMATION
(��)�̾��� ȯ���߽� ��� ��ġ�� �������� �������� ȯ�� �濵 �ý����� ��ϰ� �ֽ��ϴ�.
����ڷ�
Polarographic ��Ҽ���
����
���� �̷� �κп��� �оа� ���� ��� ���� �ٺ� ���踦 ���������Ƿ� ���� ��� ������ ��� �ϴ� ������ ���� � ���ε��� CONTROL �ؾ� �ϴ� ���� ���� �м�Ű�� �Ѵ�. ���� ������ ���¿� �־�� ���� ȭ�� �������� �ݼ��� �ֳ��(���)�� �ݼ��� ij�ҵ�(����)�� �̷���� �� �ΰ��� ������ ���� ��� ��� �ִ� �����̴�. �ϳ��� ���� ȸ�ΰ� �ֳ��� ij�ҵ忡 ����Ǿ� ������ ���ϰ� �Ǹ� ������ �ֳ��� ij�ҵ� ���̿� �帣�� �ȴ�.
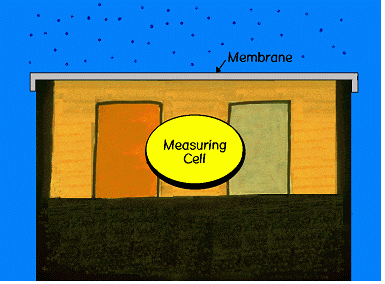
��극���� ���Ͽ� ���ؾǷ� ħ���ϴ� ��Ҵ� ���� �� ���صȴ�. �̰��� ���ؿ��� ������ ������ ���ؾ� �ǿ� ���� ����� �翡 ����Ͽ� ������ �帧�� ������ ������ ������ �����ϰ� �ȴ�. �����Ƿ� ���� ��Ҿ��� ��극�� �ܺ��� �о��̳� ����� Fugacity (�̻���) �� ����Ѵ�.

���ؾ� �ǿ����� ������ �� ���ؿ����� �������� �������� ������. ����(99.99%) �� ij�ҵ� ������ ���� ������ �Ʒ��� ȭ�� �����Ŀ� ������.
O2 + 2H2O + 4 e- -------> 4 OH -
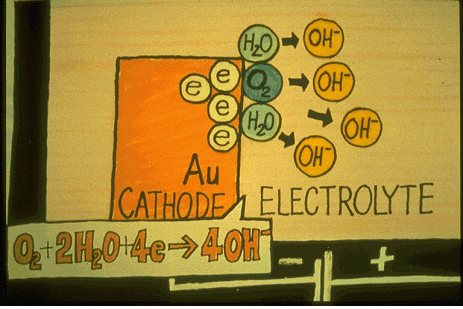
��� ���ڴ� �� ���� �ΰ��� ij�ҵ� ǥ�����κ��� ���� 4���� ���ڿ� �����Ͽ� 4���� ����� �̿��� �����Ѵ�. ij�ҵ� ���� ������ �ΰ��� ���� �ܰ�� ���� �� �ִ�.
1. ij�ҵ���� ��� �̵� 2. ij�ҵ� ǥ�鿡���� ��ȭü���� ������ �̵�
���� �� ������ �Ͼ�� ���ؼ��� ��Ұ� �ݼ� ǥ�����κ��� �� 1-2 ���� ���� (Molecular Diameters: 5x10-8 cm)�� �Ÿ��� �־�� �Ѵ�.
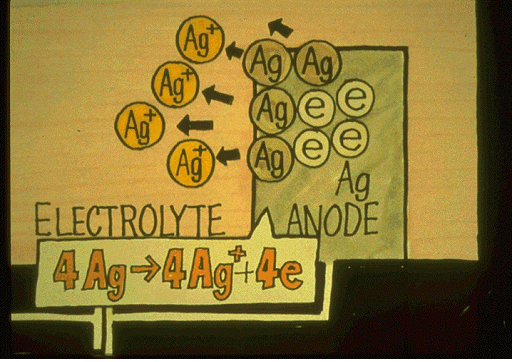
ȸ�θ� ���Ͽ� ���Ӿ��� ������ �帣���� �Ϸ��� ij�ҵ忡�� 4���� ���ڰ� �Ҹ�Ǵ� ���� �ֳ�忡 4���� ���ڸ� �����Ͽ� ������ �� �־�߸� �Ѵ�. Orbisphere�� �ֳ��� ������ �Ǿ� �־� �� ǥ�鿡�� �Ͼ�� ������ �̷��� ���� �и� ������ �ȴ�.
4AG -------> 4 AG+ + 4e-
�ֳ��� ���صǾ� �� �̿°� 4���� ���ڰ� �����ȴ�.
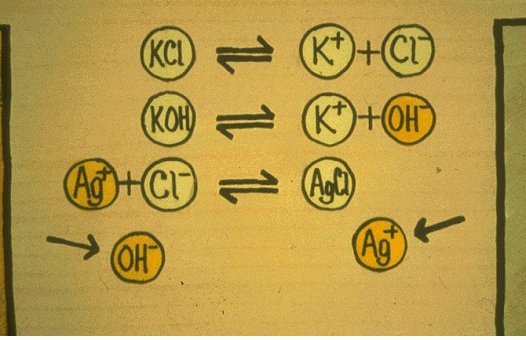
������ ������ �ݼ��� ���� ���ڿ� ���ؾ��� ���� �̿¿� ���Ͽ� ���ȴ�. ������ �̷��� �� ������ �帣�� ���� �Ű��Ѵ�. ���ؾ��� ��ȭĮ������ �Ǿ� �ִµ� ���뼺���� Į�� �̿°� ���� �̿����� �и��ȴ�. �� ������ ������ �ֳ�忡�� ���ϴ� ���̿°� �����Ͽ� �ҿ뼺�� �������� �����ϴµ� �ִ�. �̰��� �ֳ�� �αٿ��� �� �̿��� Ȱ���� �Ҵ��� �Ͽ� ij�ҵ�� Ȯ��Ǿ� ���� ���ݵǴ� ���� �����ϰ� �ȴ�. �̸��Ͽ� ������ �帧�� ���ϰ� �ǰ� �� ������ ��Ⱑ �ؼ��Ͽ� ���� ���� �ΰ� ��Ҿ����� �����س��� ���̴�. ���� �̿��� ���̿°� ������ ������ ��ȭ���� �����ǰ� �����ȴ�.
�ֳ��(���) ij�ҵ�(����) ���̿� �������� ������ ������ �����Ͽ� �ð��� ������ ��ġ �ʴ´�. ����� ����ġ�� ����Ƿ� ij�ҵ��� ���ڴ� ���� ������ ������ �ȴ�. ij�ҵ��� ǥ�鿡���� ���ڰ� O2 ���� ���� �ΰ��� H2O�� �����Ͽ� 4OH- �̿��� ����Ų��. �ֳ�忡���� ���� 4���� ���̿��� �����Ͽ� ���ؾ��� ���̿� 4���� ��ȭ��Ű�� �ݼ� �κп� 4���� ���ڸ� ���� �Ͽ� ���� ȸ�θ� �����Ѵ�. ����, �̶� ������ ������ ũ�⸦ ��� ������ �ؾ� ������ �ߴ��� �����̴�.
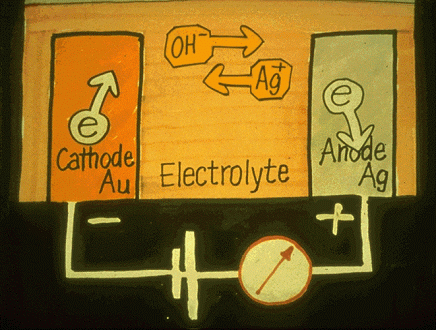
ù°�� �ֳ�尡 ������ ���� ���ٰ� ����. �̴� �ſ� ū ������ ū ���� ���� ����Ű�� �ʰ� ����� �� ������ �ǹ��Ѵ�. ���� �������� ���ϴ� ������ ���ϸ� ����� �������� ��Ÿ���� �Ѵ�. �������� ���¿����� ���ؾ� ������ �Ͼ�� Ohm�� ���� ���ϴ� ���� ������ �� �ִ� �����̴�. ���� ������ ���ϴ� ��쿡�� ���� �������� �����Ƿ� ��� ���ڿ� �����ϱ ���ġ ���Ͽ� ������ ���� ������ ��ġ �ʴ´�.
������ Ŀ���� �Ǹ� ������ �̵����� ������ʷ� �����Ͽ� ������ DIFFUSION CONTROLLED LIMIT���� �Ҹ��� �Ѱ����� �̸� ������ �����ϰ� �ȴ�. �� �̻� ������ ũ�� �Ͽ� �ָ� �ᱹ �ٽ� ������ �����ϴµ� �̴� �����ڳ� �����̿°� ���ο� ������ ������ ���Ұ����� ���� �ȴ�. ���� ���ϴ� ������ �� DIFFUSION CONTROLLED LIMIT �αٱ��� �÷� ��� ������ �����ϴµ� ����� ������ �����ϰ� �ȴ�.
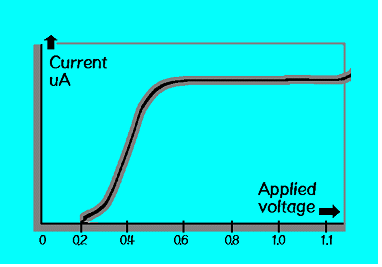
ij�ҵ� ũ��� ���� ������ ������ �������� ����� �����Ѵ�. ������ ũ�Ⱑ ũ�� ��ȣ�� �ٷ�Ⱑ ���� ���� �����ϴ�. ���� �ֳ���� �Ҹ� ���ؾ��� �Ҹ� �����Ͽ� ������ ����� �� ���̴�.���� ij�ҵ��� ���°� ��� Ȯ���� ������ �����ڸ� �κп����� ��� Ȯ������ ����Ͽ� ǥ�鿡 �������� Ȯ��Ǵ� ���� ������ �ǵ��� �����ž� �Ѵ�.
����, ���ؾװ� �������а� �Բ�, �����ؾ� �� ���� ��극���̴�. ��극���� ������ ���ؾװ� ������ ���� ����� �и���Ű�� �������� ��� ���ڸ� �귯 ����ϰ� �Ѵ�. ����α��� ��Ҽ��������� ���÷κ��� ��극���� ���� ����� ħ������ ���� ������ �����ȴ�. ���Ƿ� ��극���� ���ġ�� ������ �־� ������ ���� (Limiting Factor)���� �ۿ��Ѵ�. �������� ��극�� ���� ����� �з¿� ����Ѵ�. ��극�� ǥ�鿡�� �浹�ϴ� ���ڰ� ���� ���� ��극���� ����ϴ� ���ڼ��� ���� ���� �и��ϴ�.
�������� ��극�� ���� ����� �з¿� ����Ѵ�. ��극�� ǥ�鿡�� �浹�ϴ� ���ڰ� ���� ���� ��극���� ����ϴ� ���ڼ��� ���� ���� �и��ϴ�.
�������� ���� ��극�ο����� ����� ���ص��� ����Ѵ�. ���극�� ���� ��� ���ڰ� ����ؾ� �ϹǷ� ������� ������ ��극�ο����� ������ Ư���� ���ص��� ���� �ٸ���.
�β��� ���� ������ Ư���� �Ȱ��� �ΰ��� ��극�� �̶� ��극�ο� ���صǴ� ��Ҵ� �ٸ� �� �ִٴ� ���̴�.
�̴� �� ��극���� ��ü �Ŀ��� �ݵ�� Calibration�� �ؾ� �Ѵٴ� ���� �ǹ��Ѵ�.
�������� ������ ���극���� ����ϴ� ��� ������ Ȱ�� ���̼��� ǥ���ϴ� ��극�� ���������� ��� Ȯ�� ��� (Diffusion Coefficient)�� ����ϴ� ���̴�.
���� Ȯ�� ����� ��극���� ���� �ð��� �� ���� ��� ���ڰ� ��극���� ����Ͽ� ���ؾ� �̸��� �� ���̴�. ������, �̷��� ����� ��� �������� ������ �����ϰ� ���ϴ� �ֵ� ����̴�. Ȯ������ ������ ��극�ο� ���ص� O2�� ��극�� ���� ������ �����ϴµ� �ɸ��� �ð��� ��ٴ� ���� �����϶�. ���Ƿ�, Ȯ�� ����� ��� �������� �����ӵ��� �����ϱ �Ѵ�.
�������� ��극���� �β��� �ݺ���ϴµ� �̴� ��� ���ڰ� ������ �� �Ÿ��� ����� �ǹ��Ѵ�.
��극���� �β��� ���� ������ ���� ������ ũ�� ���� �ð��� ��극�� ������ ����� ������ ��� ���ڼ��� ����. ���� ��극�� ���ǿ��� ���� ��Ҿп� ���� ���ϴ� ������ �۾� ���� �ȴ�.
�̷��� ���� Ư������ �����Ͽ� ���� �ð��� ��극���� ����Ͽ� ������ ������ ��ҷ��� �����ϰ� �Ǵ� ���̴�.
�̷��� ��ҵ��� �Ʒ��� �����ó�� ���� �ð��� ���� ������ ����ϴ� ��� ������ ���� ������ �ش�.
Pm = PO2 Sm Dm / X m
PO2 (�з�), Sm(��극���� ��� ������), Dm(��극���� ��� Ȯ�� ���) Xm (��극���� �β�)
������ �̷��� �������ڼ��� ���� ����Ͽ� �Ʒ� ������ ǥ���� �� �ִ�.
I = ( 4 . F . A . Dm . Sm . PO2 ) / Xm
F : ���. Single Charged Ion �� 1 Mole�� ���� 4 : ��� ���� �ϳ��� ���ڰ� 4�� A : ij�ҵ� ����
������ ���� ����� �оп� ���������� ����Ѵ�. �̷��� ������ ��� ����� �ſ� ����� ���� �з��̳� ������ ū �з¿����� ����ġ �ʴ´�. ��Ҿп� ���������� ����ϴ� ������ ������ �д�. ����, ���������� ���ؾ��� ������ ����ϴ� �̿��� �帧�� ���� ���п� ��������� ������ ���� ������ Ohmic Limit ������ ���Ѵ�. �� ���¿����� �ܷ� ������ ���ڸ� ����� ���ӽ�Ű�� ���ϰ� �ȴ�.
�ܷ� ������ �ſ� �߿��� ������ ��ҷμ� ���� ������ ���ġ�� �ּ�ġ�� �����Ѵ�.
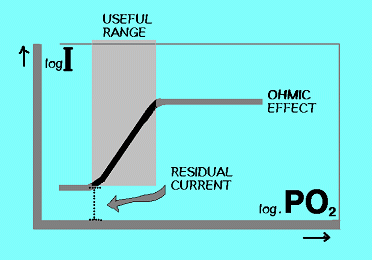
���� ������ �ּ� ���ġ�� �� �ܷ� ������ ������ ������ ��극�ΰ� ij�ҵ��� ������ Ư������ ������ �ִ�.
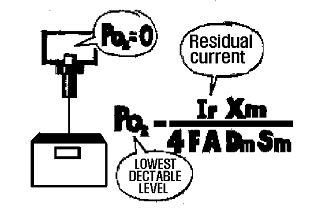
�ܷ� ������ ���� ���� ��ҿ� ���þ��� ������ �帣�� �������� ������ �ִ� ����� �����´�. ���ؾ��� ä��� �������� ������ ���ؾ� ���� ���ص� ��Ҹ� ������ ����. �̰��� ij�ҵ忡 Ȯ��Ǿ� �����ϸ� ���� ���� ��� �оп� ������� ������ ����ų ���̴�. ������ �����ϰ� �ִ� ��ü ��ü�� ��ҳ� ���κ��� ��� ��ǰ ���̷� ������ ���� ������ ��Ҵ� ���� ������ ������ �� ���̴�. ��Ÿ�� ������ ������ �ִ� �͵�μ� �ֳ��κ��� ���� ij�ҵ忡 ���ݵǴ� �� �̿��� �� �� �ִ�. �������� ���� ȭ�� �������δ� ���ؾ׳��� ���κ����� ���Ұ����� ���� ����, ���ؾ׳��� �ִ� � �Ҽ����� ���� ���ظ� �� �� �ִ�. ���������� ij�ҵ�� �ֳ�� ���̿� ������ ����ġ ���� ��쿡�� �ܷ� ���� ���� (Residual Electronic Leakage) �� ����� �Ѵ�. ������ �帧�� ��� ������ �� ������ �������̹Ƿ� �̷��� ���� �ֺ� ������ ��ǻ� ���� ��ü�� ������ �� �����ӿ��� �ұ��ϰ� ���� ���� ���� ��� �Է����μ� �����ǰ� ������ ��Ÿ���� ���̴�. �̷� �͵��� ������ ���߽�Ű�� ����ε� ���� ���ġ�� ������ ��� �ѷ��� ��Ÿ���� �͵��̴�.
